کریسپر میتواند معلولیت عضلانی را درمان کند!
دانشمندان با استفاده از فناوری ویرایش ژن توانستند دیستروفی ماهیچهای را در سگها درمان کنند که امید را برای درمان فلج عضلانی در انسان زنده کرده است.
موبنا – یک تکنیک اصلاح ژن، بافت عضلانی چهار سگ را تا ۹۲ درصد بازیابی کرد. این درصد به محققان این امیدواری را میدهد که درمان “دیستروفی ماهیچهای دوشن” (DMD) نزدیک است.
دیستروفی ماهیچهای دوشن(Duchenne muscular dystrophy) یا DMD شایعترین و شدیدترین نوع از بیماریهای دیستروفی ماهیچهای از گونه X پیوند یافته و ژنتیکی است. از عوارض اصلی این بیماری تحلیل و نابودی ماهیچههای ارادی(که در کنترل بدن نقش حیاتی دارند) است که در مواقع شدید، نهایتا منجر به عدم توانایی در راه رفتن، ۹۶ درصد معلولیت، مشکلات تنفسی و مرگ میشود.
اکنون برای اولین بار، محققان از فناوری ویرایش ژن موسوم به کریسپر(CRISPR) برای جلوگیری از پیشرفت دیستروفی ماهیچهای دوشن در یک پستاندار بزرگ استفاده کردهاند. نتایج این پژوهش اکنون هزاران کودک را در سراسر دنیا امیدوار میکند.
گروهی از محققان مرکز هامون “UT Southwestern’s for the Recenerative Science و Medicine” یک تکنیک ژنتیکی ابداع کردهاند که میتواند راه حلی برای درمان DMD ارائه دهد.
محققان با استفاده از یک تکنیک ویرایش ژن یکپارچه برای بازیابی دیستروفی در عضله تا ۹۲ درصد استفاده کردند. مطالعات قبلی نشان میدهد تنها بازیابی ۱۵ درصدی میتواند به این بیماران کمک کند.
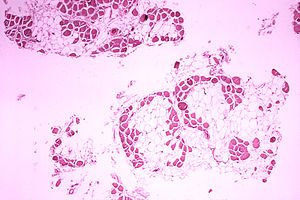
دیستروفی ماهیچهای بیماری ناشی از نقص ژنتیکی است که منجر به ضعف عضلانی، کاهش تونایی حرکت و دشواری انجام کارهای روزانه میشود.
DMD از هر ۳۵۰۰ فرد ۵ تا ۲۴ ساله، یک نفر را تحت تاثیر قرار میدهد. مردان به طور قابل توجهی بیشتر تحت تاثیر قرار میگیرند، در حالی که دختران نیز میتوانند نشانگر ژنتیکی DMD را با خود داشته باشند، اما مردان زودتر دچار نشانههای DMD میشوند و بیشتر مبتلا میشوند.
چیزی که DMD را به طور خاص مورد توجه قرار میدهد این است که ضعف عضلات در کودکان را قبل از رسیدن به ۵ سالگی شروع میکند.
دکتر “اریک اولسون”، مدیر مرکز هامون میگوید: کودکان مبتلا به DMD اغلب از دنیا میروند، زیرا قلب آنها توانایی پمپاژ خود را از دست میدهد و یا دیافراگم آنها برای نفس کشیدن بیش از حد ضعیف میشود. امیدوارم این دستاورد باعث جلوگیری از این اتفاق شود.
DMD نه تنها موجب ضعف و عدم توانایی عضلانی میشود، بلکه منجر به نارسایی قلبی در جوانان میشود. اغلب موارد مرگ و میر افراد مبتلا به DMD در اوایل دهه سوم زندگیشان است.
گروه محققان پژوهش خود را در شماره اخیر نشریه Science منتشر کردهاند که از روشی استفاده کردهاند که میتواند آنها را به سرعت در مسیر شروع آزمایشات بالینی قرار دهد.
آنها از چهار سگ استفاده کردند که دچار نوعی جهش ژنتیکی بودند که اغلب در بیماران DMD یافت میشود. محققان سپس از یک ویروس بیضرر به نام ویروس “AAV” استفاده کردند تا اجزای ویرایش شده ژنتیکی را به ژن دیستروفین تحویل دهد.
در عرض چند هفته، پروتئین از دست رفته در هر ۴ نمونه بازسازی شد. همچنین درصد بازیابی در قلب ۹۲ درصد و در دیافراگم ۵۸ بود.
دکتر “لئونلا آمواسی” نویسنده ارشد این مطالعه و مربی دستیار زیست شناسی مولکولی گفت: استراتژی ما متفاوت از دیگر روشهای درمانی برای DMD است، چرا که جهش ژنتیکی را که باعث بیماری شده را ویرایش میکند و بیان طبیعی ژن دیستروفین را بازیابی میکند. اما قبل از اینکه بتوانیم از این روش در انسان استفاده کنیم، باید آزمایشات بیشتری انجام دهیم.
نتایج این مطالعه اگرچه امیدوارکننده هستند، اما هنوز برای آزمایشات انسانی آماده نیست. محققان همچنین میخواهند اطمینان حاصل شود که عوارض جانبی برای ویرایش این ژن وجود نداشته باشد.
دکتر اولسون خاطرنشان کرد اگر همه چیز طبق برنامه پیش رود، آزمایشات بالینی طی چند سال آتی میتواند انجام شود.
فراوانی دوشن ۱ در هر ۳۵۰۰ کودک پسر است. این بیماری در اثر تغییرات و نقض در ژن DMD واقع در کروموزوم X ایجاد میشود. این ژن مسئول ساخت پروتئین دیستروفین، مادهای ضروری برای حفظ و ثبات ماهیچهها است و در غشای سلولی قرار دارد.
بهطور کلی بانوان دارای کروموزوم X ناقص و حامل این بیماری هستند و میتوانند این بیماری را به نیمی از فرزندان پسر خود منتقل کنند. ناقص بودن یکی از کروموزومهای X در بانوان غالبا ارثی یا ممکن است در اثر جهشهای ژنتیکی باشد.
بهطور کلی علایم بیماری در ۶ سالگی ظاهر میشود، گرچه در دوران نوزادی هم نمایان است. نوزاد در موقع تولد کاملا سالم به نظر میرسد، ولی هنگامی که شروع به حرکت میکند، حتی زمانی که با چهار دست و پا یا سینهخیز میرود، حرکت او کندتر از همسالان خود است و زود به زود خسته میشود.
هنگامی که کودک به راه میافتد، ضعف ماهیچهای به تدریج واضحتر میشود. معمولا والدین نسبت به نحوه راه رفتن غیرطبیعی یا اشکال در برخاستن فرزندشان از روی زمین، راحت زمینخوردن، اشکال در بالا رفتن از پلهها و عدم توانایی دویدن یا انجام حرکات ورزشی در مقایسه با همسالانشان نگران میشوند.
بزرگ شدن غیرطبیعی ماهیچههای ساق پا و ضعف خفیف تا متوسط ماهیچههای ابتدای اندام تحتانی، به صورت راه رفتن اردکوار و عدم توانایی در برخاستن راحت از روی زمین تظاهر میکنند.
این کودکان بهطور مشخص برای برخاستن از حالت نشسته از دستها و بدنشان کمک میگیرند که به نشانه گاور (Gowers’ sign) معروف است.
تحلیل ماهیچهای به صورتی است که در ۸ سالگی ضعف ماهیچهها کاملا بارز میشود. این تحلیل ماهیچهای ابتدا از پاها و لگن شروع، باعث کاهش حجم و نابودی ماهیچههای این ناحیه میشود و نهایتا دستها، بازوها و شانه را نیز در بر میگیرد که موجب افتادگی شانه میشود.
بیمار در ۱۰ سالگی توانایی راه رفتن را از دست میدهد و به ویلچر نیاز پیدا میکند. از آنجایی که دو سوم از وزن بدن از ماهیچهها تشکیل شده است، با نابودی ماهیچهها وزن بدن به شدت کاهش مییابد و به یک سوم از کل آن میرسد.
در بیشتر مواقع پیشرفت بیماری ادامه مییابد و به علت رشد غیرطبیعی استخوانهای ستون فقرات، ستون فقرات به صورت حرف S انحنا پیدا میکند و قفسه سینه اندکی تغییر شکل میدهد که سبب جمع شدگی بدن میشود.
پیشرفت بیماری در مواقع شدید نهایتا با مشکلات تنفسی و مرگ همراه خواهد بود. طول عمر متوسط برای بیماران مبتلا به DMD معمولا بین ۲۰ تا ۳۰ سال است.
این تحقیق در مجله Science منتشر شده است.
منبع: ایسنا